 Bijdrage ingezonden door Menno Loos, Masterstudent UvA. Op woensdag 9 december vond de jaarlijkse octrooirecht jurisprudentielunch plaats, georganiseerd door deLex. Prof. Mr. W.A. Hoyng en Mr. B.J. van den Broek bespraken met de aanwezige advocaten en octrooigemachtigden (en een enkele student) de meest belangrijke octrooirechtjurisprudentie van 2015. Bijna veertig uitspraken passeerden de revue.
Bijdrage ingezonden door Menno Loos, Masterstudent UvA. Op woensdag 9 december vond de jaarlijkse octrooirecht jurisprudentielunch plaats, georganiseerd door deLex. Prof. Mr. W.A. Hoyng en Mr. B.J. van den Broek bespraken met de aanwezige advocaten en octrooigemachtigden (en een enkele student) de meest belangrijke octrooirechtjurisprudentie van 2015. Bijna veertig uitspraken passeerden de revue.
De zaken die verreweg het meeste stof deden opwaaien, betroffen de zaken over ‘second medical use claims’. Dit zijn conclusies die een nieuwe toepassing van een bestaand medicijn beschermen. De nieuwheid van de uitvinding is gelegen in de toepassing van het medicijn: voor een nieuwe indicatie, nieuwe subpopulatie, in een nieuwe toedieningsvorm, in een nieuw doseringsregime, of met een nieuw technisch effect.
Onder de invloed van personalized medicine zal het aantal second medical use uitvindingen in de toekomst sterk toenemen. Het is daarom van groot belang dat deze second medical use claims ook daadwerkelijk te handhaven zijn, of dat in elk geval duidelijk is hoe er met dergelijke claims moet worden omgegaan.
In deze bijdrage bespreek ik de uitspraken van het geding tussen Novartis en Sun (IEF 13841, IEF 14599, IEF 15451), waarin de moeilijkheid van handhaven van second medical use claims aan bod komt. Vervolgens bespreek ik twee mogelijke manieren hoe de rechter met second medical use claims om kan gaan.
Novartis v Sun
Novartis is houdster van een Europees octrooi op het gebruik van zoledroninezuur voor de behandeling van osteoporose (botaandoening). De uitvinding is vastgelegd in een Swiss-claim: “gebruik van zoledroninezuur voor de vervaardiging van een geneesmiddel voor de behandeling van osteoporose (…)” Zoledroninezuur werkt niet alleen ter behandeling van osteoporose, maar ook voor de behandeling van de (zeldzame) ziekte van Paget. Het product van Novartis (Aclasta) wordt voor 97,3% gebruikt voor osteoporose en voor 2,7% voor Paget.
Nu de stof zoledroninezuur en het gebruik van de stof ter behandeling van Paget niet langer beschermd zijn, staat het andere fabrikanten in elk geval vrij om de stof te gebruiken ter vervaardiging van een medicijn ter behandeling van Paget Sun brengt een generiek geneesmiddel met zoledroninezuur op de markt en heeft een marktvergunning die ziet op het gebruik van het product voor beide indicaties. Op verzoek van Sun schrapt het College ter Beoordeling van Geneesmiddelen de indicatie osteoporose uit de Summary of Product Characteristics (SmPC) en de fysieke bijsluiter (niet uit de digitale versie). Vervolgens gaat Sun een overeenkomst aan met verzekeraar VGZ waarbij wordt overeengekomen dat Sun’s zoledroninezuur het ‘preferente’ zoledroninezuur wordt, zonder een beperking m.b.t. de indicatie. Dit betekent dat als zoledroninezuur wordt voorgeschreven, VGZ alleen het product van Sun vergoedt, ongeacht de indicatie (Paget of osteoporose). Als gevolg wordt het product van Sun in grote hoeveelheden gebruikt voor de geoctrooieerde indicatie.
KG – 1e aanleg
In kort geding wordt Sun aangesproken door Novartis wegens indirecte inbreuk (aanbieden en leveren van een geneesmiddel met zoledroninezuur voor de behandeling van osteoporose). De voorzieningenrechter wijst de vorderingen af wegens serieuze kans op nietigheid (IEF 13841 12 mei 2014).
KG – beroep
In beroep vernietigt het Hof dit vonnis (IEF 14599 27 januari 2015). Het Hof oordeelt dat de uitvinding nieuw, inventief en nawerkbaar is. Bovendien komt het Hof tot het oordeel dat Sun indirecte inbreuk heeft gepleegd door het aanbieden en leveren van haar product. Het Hof overweegt, zonder dit toe te lichten, dat het product van Sun een wezenlijk bestanddeel van de uitvinding van Novartis is (r.o. 4.31). En gezien hetgeen overeengekomen tussen Sun en VGZ (zonder enige beperking m.b.t. indicaties), moest Sun weten dat haar product ook zal worden gebruikt voor de geoctrooieerde indicatie (r.o. 4.32-37). Sun heeft VGZ er nog op gewezen dat Novartis octrooi heeft op toepassing voor de behandeling van osteoporose, maar verbond hier geen leveringsconsequenties aan. Ook de e-mail die Sun aan groothandels verstuurde waarin zij op het octrooi van Novartis wees, helpt haar niet. Conclusie: indirecte inbreuk.
Bodemvonnis
Naast het kort geding is ook een bodemprocedure aanhangig, waarin Sun vernietiging vordert van het octrooi en Novartis in reconventie een inbreukverbod vordert. De rechtbank volgt het oordeel van het Hof m.b.t. de geldigheid (het octrooi is geldig), maar komt tot het oordeel dat er geen sprake is van indirecte inbreuk (IEF 15451 25 november 2015).
De rechtbank overweegt dat de Swiss-claim moet worden aangemerkt als een werkwijzeconclusie die de vervaardiging van een geneesmiddel beschermt (4.49, 4.54). Het volgt uit de uitspraak T 1780/12 (par. 22) van de Technische Kamer van Beroep dat een Swiss-claim een andere (beperktere) beschermingsomvang heeft dan een EPC2000-claim. Onder het vernieuwde Europees Octrooiverdrag (EPC2000), biedt artikel 54 lid 5 de mogelijkheid om een tweede of verdere medische toepassing van een bestaand medicijn te beschermen. Dit kan in de vorm van een use-claim (Use of substance X for treatment of Z.). Een dergelijke conclusie moet worden aangemerkt als een doelgebonden productconclusie, terwijl een Swiss-claim moet worden gezien als een doelgebonden werkwijzeconclusie.
Omdat de conclusie van Novartis een werkwijzeconclusie betreft, kan volgens de rechtbank het zinsdeel ‘voor toepassing van de geoctrooieerde uitvinding’, zoals verwoordt in artikel 73 ROW, niet anders worden begrepen dan het bereiden van het geneesmiddel zoledroninezuur voor de behandeling van osteoporose (r.o. 4.54). Het product dat Sun levert betreft een ready to use product. Dit betekent dat nergens in de keten na levering van het product bereidingshandelingen plaatsvinden. Het product van Sun dient dus niet voor toepassing van de geoctrooieerde uitvinding. De levering van het product van Sun levert dan ook geen indirecte inbreuk op. De rechtbank zegt hiermee dat een ready to use product niet kan worden aangemerkt als een wezenlijk bestanddeel van een uitvinding vastgelegd in een Swiss-claim.
Directe inbreuk?
Kan het leveren van Sun’s generiek worden aangemerkt als directe inbreuk door Sun? De rechtbank houdt vanwege ontwikkelingen die kort voor de mondelinge behandeling hebben plaatsgevonden (het arrest in kortgeding en uitspraken in de vergelijkbare Engelse zaak Warner-Lambert v Actavis) haar uitspraak hierover vooralsnog aan. De rechtbank sluit het echter niet uit dat er sprake is van directe inbreuk, d.m.v. het aanbieden en leveren van een rechtstreeks verkregen voortbrengsel van de werkwijze (art. 53 lid 1 sub b ROW).
Wat mij betreft heeft de rechter bij de beoordeling of sprake is van directe inbreuk twee mogelijkheden: een strikte grammaticale interpretatie, of een meer pragmatische benadering.
Strikte grammaticale interpretatie
Directe inbreuk kan volgens een grammaticale interpretatie van de Swiss-claim alleen bewezen worden als de generiekfabrikant daadwerkelijk alle stappen van de claim heeft doorlopen of het voortbrengsel het gevolg hiervan is. Dus de volgende vraag moet worden gesteld: heeft Sun zoledroninezuur gebruikt voor de vervaardiging van een geneesmiddel voor de behandeling van osteoporose? Vast staat dat Sun zoledroninezuur heeft gebruikt, en ook dat dit gebruikt is om een geneesmiddel te vervaardigen. Maar is dit geneesmiddel vervaardigd voor de behandeling van osteoporose? Uit Engelse rechtspraak blijkt dat deze vraag neerkomt op een debat over de invulling van het woord ‘voor’. Bij een strikte grammaticale interpretatie van de Swiss-claim moet worden geconcludeerd dat de beweerdelijk inbreukmaker al bij het gebruik van de stof voor het vervaardigen van een geneesmiddel de bedoeling moet hebben gehad dit geneesmiddel voor de geclaimde indicatie te gebruiken. Judge Arnold gebruikt in Warner-Lambert v Actavis I het criterium van ‘subjective intention’, een term die zich volgens mij het best laat vertalen als ‘expliciete intentie’. De intentie van de fabrikant is meestal echter pas kenbaar op het moment dat het product op de markt komt. Omstandigheden die in overweging genomen dienen te worden om de intentie van de fabrikant te ontwaren zijn: het label waaronder het product wordt verkocht (is de beschermde indicatie geschrapt?), verdere vermeldingen op de verpakking (staat op grote verpakkingen bestemd voor groothandelaren vermeld dat het product niet bestemd is voor de beschermde indicatie?), overige maatregelen ter voorkoming van gebruik van het generiek voor de beschermde indicatie (heeft de fabrikant waarschuwingsbrieven gestuurd naar groothandelaren en apothekers?) en overige omstandigheden (is fabrikant een overeenkomst aangegaan, onbeperkt m.b.t indicaties?; hoe verhouden de verkoopcijfers van de beschermde en de vrije indicatie zich tot elkaar?).
In de onderhavige casus heeft Sun haar product op de markt gebracht onder een skinny-label (de beschermde indicatie was geschrapt), ook heeft zij VGZ en groothandelaren op de hoogte gesteld van het octrooi van Novartis. Deze acties geven in sterkere mate aan wat niet de intentie is van Sun, dan dat de deelname in de onbeperkte overeenkomst met VGZ aangeeft wat wel de intentie is van Sun. Weliswaar nemen deze acties niet weg dat het voor Sun voorzienbaar had kunnen zijn dat haar product voor de beschermde indicatie gebruikt zou kunnen worden, maar de acties geven wel voldoende blijk van haar expliciete intentie het product alleen voor de ziekte van Paget op de markt te brengen. Volgens deze strikte benadering kan dus geen directe inbreuk worden bewezen.
In de praktijk zal het nauwelijks voorkomen dat een generiekfabrikant geen carve-out toepast of geen maatregelen treft, zodat niet bewezen kan worden dat de fabrikant expliciete intentie heeft zijn product voor de beschermde indicatie te verkopen. Deze strikte benadering zal daarom tot gevolg hebben dat een tweede medische indicatie-claim verwordt tot een tweederangs recht; onmogelijk te handhaven.
Een meer pragmatische benadering
De bovenstaande benadering is een nadelige voor octrooihouders. Er zou daarom ook gepleit kunnen worden voor een andere invulling van het ‘intentiecriterium’, onderliggend aan het woord ‘voor’. Het intentiecriterium moet ruimer worden opgevat: de generiekfabrikant heeft een redelijke verantwoordelijkheid om er voor te zorgen dat zijn product niet voor de beschermde indicatie wordt gebruikt. In het geval dat een niet verwaarloosbaar aantal van zijn product toch voor de beschermde indicatie wordt gebruikt, dan heeft de generiekfabrikant geen afdoende maatregelen getroffen dit te voorkomen, en heeft hij kennelijk de intentie gehad een medicijn te vervaardigen voor de behandeling van de beschermde indicatie.
Een dergelijke invulling van het intentiecriterium komt de facto neer op een verruiming van de beschermingsomvang van een Swiss-claim: van die van een doelgebonden werkwijzeconclusie, naar die van een doelgebonden productconclusie.
Het Hof heeft in haar arrest van 27 januari 2015 wellicht gedacht dat de constructie van de Swiss-claim gezien moet worden als een ‘trucje’ van de GKvB (G 5/83) om uitvinders van tweede medische toepassingen tenminste enige bescherming te bieden, in tijden dat het EOV nog niet voorzag in de bescherming van tweede of verdere medische toepassingen (1984). En misschien heeft zij daarin gelijk. Aangezien het EOV nu wel voorziet in bescherming van tweede medische toepassingen, is dit trucje niet meer nodig en kunnen Swiss-claims net als EPC2000-claims worden behandeld. Deze pragmatische benadering volgend, moet geconcludeerd worden dat Sun in de onderhavige casus zowel directe inbreuk als indirecte inbreuk pleegt. Nu de beschermingsomvang zich ook uitstrekt tot het gebruik van het geneesmiddel (en niet alleen tot de vervaardiging ervan), vormt het generieke zoledroninezuur namelijk een wezenlijk bestanddeel van de uitvinding. Levering van het generieke zoledroninezuur levert daarom een indirecte inbreuk op.
In elk geval zou de pragmatische benadering een einde maken aan de rechtsonzekerheid over de (on)mogelijkheid van handhaving van Swiss-claims (want goed mogelijk). Een groot probleem van deze benadering, dat hoe dan ook bij EPC2000-claims speelt, is dat generiekfabrikanten aanzienlijke maatregelen moeten treffen om te voorkomen dat hun product voor de beschermde indicatie gebruikt zal worden, met eventueel hogere prijzen tot gevolg en in het ergste geval een kleiner aanbod van generieke middelen. Aangezien onder het huidige regulatoire stelsel, medicijnen op basis van stofnaam zonder vermelding van de indicatie worden voorgeschreven, is het niet ongebruikelijk dat een generiek aan een patiënt wordt gegeven voor een indicatie die nog beschermd wordt door een second medical use claim. Deze praktijk in combinatie met de ruime invulling van het intentiecriterium maakt het haast onmogelijk voor generieken om de markt te betreden, omdat er altijd een risico is dat hun product wordt gebruikt voor een beschermde indicatie, waardoor de generiekfabrikant indirecte inbreuk verweten kan worden. Dit heeft zeer onwenselijke gevolgen, daarom zal óf het regulatoire stelsel m.b.t. het voorschrijven en uitgeven van medicijnen moeten worden aangepast, óf een strikter criterium voor inbreuk moeten worden gebezigd, zoals het criterium van expliciete intentie.
Het is evident dat beide benaderingen een onbevredigende uitkomst hebben. Een strikte benadering heeft tot gevolg dat het bijna onmogelijk is om inbreuk te bewijzen, waardoor een second medical use claim waardeloos wordt. Een pragmatische benadering heeft tot gevolg dat inbreuk gemakkelijk te bewijzen is, maar breidt de beschermingsomvang van een Swiss-claim uit en zadelt generiekfabrikanten op met een enorme verantwoordelijkheid.
De moeilijkheid van handhaven van second medical use claims staat in direct verband met het huidige regulatoire stelsel dat geen rekening houdt met het octrooirecht. In combinatie met een preferentiebeleid van een verzekeraar lijkt het zelfs inbreuken te faciliteren. Het staat daarom buiten kijf dat het ‘voorschrijf- en uitgeef’-stelsel aanpassing behoeft. Een nieuw systeem moet er voor zorgen dat in het geval een middel wordt voorgeschreven voor een indicatie die is beschermd door een second medical use claim, de apotheker alleen maar het medicijn van de octrooihouder kan uitgeven. Als een middel wordt voorgeschreven voor een off-patent indicatie, staat het de apotheker vrij een medicijn te kiezen.
Ik ben van mening dat, zolang het stelsel niet is aangepast, de mankementen van het huidige stelsel niet op het bord moeten komen van de generiekfabrikant (Sun in dit geval). Als de pragmatische benadering gehanteerd zal gaan worden, dan verwacht ik namelijk dat minder generieken de markt zullen betreden. Weliswaar vinden er dan minder inbreuken plaats, maar er zullen ook veel minder medicijnen beschikbaar zijn voor off-patent indicaties. Al met al vind ik dat het belang van toegang tot goede (en betaalbare) gezondheidszorg moet prevaleren boven het (financiële) belang van octrooihouders, waardoor, zolang het huidige stelsel van kracht is, rechters het strikte expliciete intentiecriterium moeten bezigen bij de beoordeling of sprake is van inbreuk.
Menno Loos


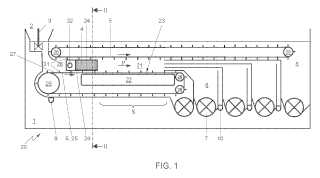 Octrooirecht. Urban Mining Corp is rechthebbende op het Nederlandse octrooi
Octrooirecht. Urban Mining Corp is rechthebbende op het Nederlandse octrooi  The
The  Bijdrage ingezonden door Arnoud Engelfriet,
Bijdrage ingezonden door Arnoud Engelfriet,  Bijdrage ingezonden door Menno Loos,
Bijdrage ingezonden door Menno Loos,  The Unified Patent Court
The Unified Patent Court The European Parliament (...) having regard to the decision of the Enlarged Board of Appeal of the European Patent Office (EPO) of 25 March 2015 in Cases G2/12 (on tomatoes) and G2/13 (on broccoli), [red.
The European Parliament (...) having regard to the decision of the Enlarged Board of Appeal of the European Patent Office (EPO) of 25 March 2015 in Cases G2/12 (on tomatoes) and G2/13 (on broccoli), [red.  Van de
Van de  Bijdrage ingezonden door Cees Mulder,
Bijdrage ingezonden door Cees Mulder, 























































































